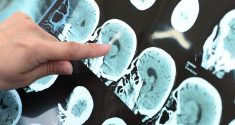
Die Alzheimer-Krankheit bringt oft die täglichen Gewohnheiten einer Person durcheinander. Schlafstörungen, unruhiges Hin- und Herwälzen und häufige Nickerchen am Tag sind häufige Frühwarnzeichen. In späteren Stadien leiden Patienten häufig unter „Sundowning“, einer Phase erhöhter Verwirrung und Unruhe, die tendenziell gegen Abend auftritt. Diese Muster deuten auf einen engen Zusammenhang zwischen dem Fortschreiten der Alzheimer-Krankheit und dem circadianen System hin – der inneren Körperuhr, die Schlaf, Wachsein und andere tägliche biologische Zyklen reguliert. Bis vor kurzem war Wissenschaftlern jedoch nicht vollständig klar, wie tief dieser Zusammenhang tatsächlich ist.
82 Gene, die mit dem Risiko einer Alzheimer-Erkrankung assoziiert werden
 Ein Forscherteam der Washington University School of Medicine in St. Louis hat nun anhand von Mausmodellen nachgewiesen, dass die Alzheimer-Krankheit den circadianen Rhythmus in bestimmten Gehirnzellen stört. Diese Störung verändert, wie und wann Hunderte von Genen ein- und ausgeschaltet werden, und verändert damit wichtige Prozesse, die zur ordnungsgemäßen Funktion des Gehirns beitragen. Ihre Ergebnisse, die in Nature Neuroscience veröffentlicht wurden, legen nahe, dass die Wiederherstellung oder Stabilisierung dieser inneren Rhythmen einen neuen Ansatz für die Behandlung von Alzheimer eröffnen könnte.
Ein Forscherteam der Washington University School of Medicine in St. Louis hat nun anhand von Mausmodellen nachgewiesen, dass die Alzheimer-Krankheit den circadianen Rhythmus in bestimmten Gehirnzellen stört. Diese Störung verändert, wie und wann Hunderte von Genen ein- und ausgeschaltet werden, und verändert damit wichtige Prozesse, die zur ordnungsgemäßen Funktion des Gehirns beitragen. Ihre Ergebnisse, die in Nature Neuroscience veröffentlicht wurden, legen nahe, dass die Wiederherstellung oder Stabilisierung dieser inneren Rhythmen einen neuen Ansatz für die Behandlung von Alzheimer eröffnen könnte.
„Es gibt 82 Gene, die mit dem Risiko einer Alzheimer-Erkrankung in Verbindung gebracht werden, und wir haben festgestellt, dass der circadiane Rhythmus die Aktivität von etwa der Hälfte dieser Gene steuert“, sagte Dr. med. Erik S. Musiek, PhD, Charlotte & Paul Hagemann-Professor für Neurologie an der WashU Medicine, der die Studie leitete. Bei Mäusen, die als Modell für die Krankheit gezüchtet wurden, folgten diese Gene nicht mehr ihren üblichen täglichen Mustern. „Das Wissen, dass viele dieser Alzheimer-Gene durch den circadianen Rhythmus reguliert werden, gibt uns die Möglichkeit, Wege zu finden, um therapeutische Behandlungen zu identifizieren, mit denen sie manipuliert und das Fortschreiten der Krankheit verhindert werden können.“
Die Belastung durch Schlafstörungen
Musiek, der das Center on Biological Rhythms and Sleep (COBRAS) an der WashU Medicine mitleitet und sich auf Alterung und Demenz spezialisiert hat, stellte fest, dass Schlafstörungen eines der häufigsten Probleme sind, über die Pflegekräfte von Alzheimer-Patienten berichten. Seine früheren Arbeiten zeigten, dass Schlafveränderungen bereits Jahre vor dem Auftreten von Gedächtnisverlust beginnen. Über die Erschöpfung von Patienten und Pflegekräften hinaus verursachen diese Störungen Stress, der das Fortschreiten der Krankheit beschleunigen kann. Um diesen Kreislauf zu durchbrechen, müsse man zunächst herausfinden, wo er beginnt. Das circadiane System des Körpers reguliert etwa 20 % aller Gene im menschlichen Genom und steuert lebenswichtige Prozesse wie Verdauung, Immunantwort und Schlaf-Wach-Zyklen.
In früheren Forschungen identifizierte Musiek ein Protein namens YKL-40, das im Laufe des Tages natürlichen Schwankungen unterliegt und dabei hilft, den normalen Amyloidspiegel im Gehirn zu regulieren. Zu viel YKL-40, das mit dem Alzheimer-Risiko beim Menschen in Verbindung gebracht wird, kann die Ansammlung von Amyloid auslösen – einem klebrigen Protein, das Plaques bildet, eines der Kennzeichen der Krankheit.
Die Wirkung von Amyloid auf die Zeitmessmechanismen des Gehirns
Da die Symptome von Alzheimer einem sich täglich wiederholenden Muster folgen, vermutete das Team, dass möglicherweise weitere circadian regulierte Proteine und Gene beteiligt sind. In der neuen Studie untersuchten sie die Genaktivität im Gehirn von Mäusen, bei denen sich Amyloidablagerungen gebildet hatten, sowie in gesunden jungen Mäusen und älteren Mäusen ohne Plaques. Über einen Zeitraum von 24 Stunden wurden alle zwei Stunden Proben entnommen, um zu verfolgen, wie sich die Genexpression im Laufe des circadianen Zyklus veränderte.
Die Forscher fanden heraus, dass Amyloidablagerungen den normalen Rhythmus von Hunderten von Genen in zwei wichtigen Arten von Gehirnzellen – Mikroglia und Astrozyten – störten. Mikroglia fungieren als Immunzellen des Gehirns und beseitigen Abfallstoffe und schädliche Substanzen, während Astrozyten die Kommunikation zwischen Neuronen unterstützen und deren gesunde Funktion aufrechterhalten. Viele der betroffenen Gene sind normalerweise für die Fähigkeit der Mikroglia verantwortlich, Abfallstoffe, darunter auch Amyloid, zu entfernen. Obwohl diese Gene nicht vollständig ausgeschaltet waren, gerieten ihre übliche Reihenfolge und ihr zeitlicher Ablauf durcheinander, wodurch das koordinierte System des Gehirns zur Entfernung von Giftstoffen geschwächt wurde.
Neue Rhythmen und potenzielle Therapien
Die Studie zeigte auch, dass Amyloid-Plaques offenbar neue rhythmische Muster in Genen erzeugten, die normalerweise keinem täglichen Zyklus folgen. Viele dieser Gene sind an Entzündungen oder der Reaktion des Gehirns auf Stress und Ungleichgewichte beteiligt. Laut Musiek deuten diese Entdeckungen darauf hin, dass Therapien, die auf die Anpassung der circadianen Rhythmen in Mikroglia und Astrozyten abzielen, eine gesündere Gehirnaktivität unterstützen könnten.
„Es gibt noch viel, was wir verstehen müssen, aber entscheidend ist, dass wir versuchen, die Uhr auf irgendeine Weise zu manipulieren, sie zu stärken, zu schwächen oder in bestimmten Zelltypen auszuschalten“, sagte er. „Letztendlich hoffen wir zu lernen, wie wir das circadiane System optimieren können, um die Amyloid-Ablagerung und andere Aspekte der Alzheimer-Krankheit zu verhindern.“